Séléniure de mercure
| Séléniure de mercure | |||
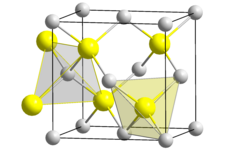 | |||
| __ Hg2+ __ Se2− Structure cristalline du séléniure de mercure | |||
| Identification | |||
|---|---|---|---|
| No CAS | 20601-83-6 | ||
| No ECHA | 100.039.903 | ||
| No CE | 243-910-5 | ||
| PubChem | 88609 | ||
| SMILES | [Se]=[Hg] PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/Hg.Se Std. InChIKey : YQMLDSWXEQOSPP-UHFFFAOYSA-N | ||
| Apparence | solide gris inodore[1] | ||
| Propriétés chimiques | |||
| Formule | HgSe | ||
| Masse molaire[2] | 279,55 ± 0,05 g/mol Hg 71,76 %, Se 28,25 %, | ||
| Propriétés physiques | |||
| T° fusion | 600 à 650 °C[1] | ||
| Masse volumique | 8,266 g/cm3[1] | ||
| Cristallographie | |||
| Système cristallin | cubique | ||
| Classe cristalline ou groupe d’espace | (no 216) cubique Hermann-Mauguin : | ||
| Précautions | |||
| SGH[1] | |||
   Danger H301 : Toxique en cas d'ingestion H330 : Mortel par inhalation H360Df : Peut nuire au fœtus. Susceptible de nuire à la fertilité. H373 : Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H410 : Très toxique pour les organismes aquatiques, entraîne des effets à long terme P264 : Se laver … soigneusement après manipulation. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin. P301+P330+P331 : En cas d'ingestion : rincer la bouche. NE PAS faire vomir. P304+P340 : En cas d'inhalation : transporter la victime à l’extérieur et la maintenir au repos dans une position où elle peut confortablement respirer. | |||
| NFPA 704[1] | |||
0 4 0 | |||
| Transport[1] | |||
Numéro ONU : 2025 : COMPOSÉ DU MERCURE, SOLIDE, N.S.A. à l’exception du chlorure mercureux et de cinabre Classe : 6.1 Étiquette :  6.1 : Matières toxiques Emballage : Groupe d'emballage II : matières moyennement dangereuses ; | |||
| Composés apparentés | |||
| Autres cations | Séléniure de zinc Séléniure de cadmium | ||
| Autres anions | Oxyde de mercure(II), Sulfure de mercure(II) Tellurure de mercure | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le séléniure de mercure, ou séléniure de mercure(II), est un composé chimique de formule HgSe. Il se présente sous la forme d'un solide gris anthracite de structure blende aux cristaux brillants d'apparence métallique. Il existe dans le milieu naturel sous la forme d'un minéral appelé tiemannite.
Sa structure cristalline appartient au système cubique, groupe d'espace F43m (no 216), avec comme paramètre cristallin a = 607 pm[3]. Il adopte une structure de type cinabre à partir de 0,75 GPa, puis halite à partir de 16 GPa et du système tétragonal au-dessus de 28 GPa[4].
Il peut être obtenu par une réaction en plusieurs étapes d'acide nitrique HNO3 avec du sélénium, de l'oxyde de mercure(II) HgO et du sulfate d'hydrazine N2H6SO4[5] :
- 3 HgO + 3 Se + 4 HNO3 ⟶ 3 HgSeO3 + 4 NO + 2 H2O ;
- 2 HgSeO3 + 3 N2H6SO4 + 6 NH3 ⟶ 2 HgSe + 3 N2 + 3 (NH4)2SO4 + 6 H2O.
Il est également possible de procéder à partir des éléments à environ 600 °C :
- Hg + Se ⟶ HgSe.
Ses propriétés électroniques sont celles d'un semimétal.
Notes et références
- ↑ a b c d e et f « Fiche du composé Mercury(II) selenide, 99.999% (metals basis) », sur Alfa Aesar (consulté le ).
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Otfried Madelung, Semiconductors: data handbook, Springer, Berlin Heidelberg, 2004, p. 239. (ISBN 978-3-540-40488-0)
- ↑ (en) Sadao Adachi, Handbook on physical properties of semiconductors, Kluwer Academic Publishers, 2004, p. 420 sqq. (ISBN 978-1-4020-7820-0)
- ↑ (de) Georg Brauer, en collaboration avec Marianne Baudler, Handbuch der Präparativen Anorganischen Chemie, 3e éd. révisée, vol. 2, Ferdinand Enke, Stuttgart, 1978, p. 1057. (ISBN 3-432-87813-3)
v · m | |
|---|---|
| Séléniures Se(-II) | |
| Se(0,I) |
|
| Se(I) |
|
| Se(II) |
|
| Se(IV) |
|
| Se(VI) |
|
v · m Composés du mercure | |||
|---|---|---|---|
| Hg(I) |
| ||
| Hg(II) |
| ||
| Hg(IV) |
| ||
 Portail de la chimie
Portail de la chimie













