マクスウェル分布
| 確率密度関数 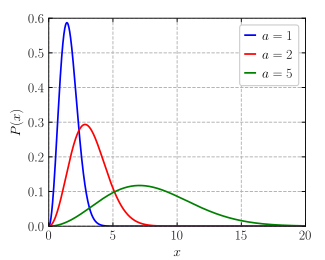 | |
| 累積分布関数  | |
| 母数 | |
|---|---|
| 台 | |
| 確率密度関数 | |
| 累積分布関数 | erfは誤差関数 |
| 期待値 | |
| 最頻値 | |
| 分散 | |
| 歪度 | |
| 尖度 | |
| エントロピー | |
| テンプレートを表示 | |
マクスウェル分布(マクスウェルぶんぷ、英: Maxwell distribution[1])とは、熱力学的平衡状態において、気体分子の速度が従う分布関数である。マクスウェル=ボルツマン分布(英: Maxwell–Boltzmann distribution[1])と呼ばれることもある。気体分子運動論により導かれたが、より一般化されたボルツマン分布からも導かれる。イギリスの物理学者J.C.マクスウェルが1859年に見いだしたことにちなんで名付けられた。
導出
気体分子運動論では、成分を vx, vy, vz とする速度ベクトル v について、x 方向の速度成分 vx の分布は、分子の質量を m、ボルツマン定数を k、絶対温度を T、係数を A として
に従うことが知られており、この式は左右対称なつりがね状の正規分布になる。したがって、係数 A を求めるには vx に関して積分した値が1になれば良いので[2][3]
より、A = √m / 2πkT となる。したがって、x 方向の速度成分 vx の分布は
また、x, y, z 方向の各速度の分布は互いに独立で、
が成り立つので、方向を指定しない3次元の速さ v の分布は
となる[2]。ここで、dvxdvydvz は半径 v で厚さ dv の球殻の体積に相当するので、4πv2dv となり[5][3]、またスカラー量である速さ v の大きさは v = √v 2
x + v 2
y + v 2
z なので、マクスウェル分布は
より
マクスウェル分布は一般化ガンマ分布(英語版)の一つである。
速度分布

分子の質量が大きく温度が低いほど分布は密になり、分子の質量が小さく温度が高いほど分布は疎になる。
導かれる速度
マクスウェル分布からは3種類の速度が導出される。
まず1つ目の速度が英語で"The most probable speed"と呼ばれる速度で、日本語では「最大確率速度[3]」や「最確速度[5][7]」などと呼ばれるものであり、記号で vmp と表される。これは、マクスウェル分布の最頻値であり、グラフのピークを求めれば良いので[5]
より[8]
次に求められる速度が平均速度 v である。これはマクスウェル分布の期待値なので
最後に求められる速度が根二乗平均速度 vrms である。これはマクスウェル分布のモーメントなので
となる[8]。
また、これら3つの速度の比は
と表される[9]。
脚注
- 出典
- ^ a b 『学術用語集』
- ^ a b c 『アトキンス物理化学』 p.27
- ^ a b c d 『理工系学生のための化学基礎』 p.17
- ^ a b 『化学・生命科学系のための物理化学』 p.28
- ^ a b c d e f 『アトキンス物理化学』 p.28
- ^ 『アトキンス物理化学』 p.26
- ^ 『化学・生命科学系のための物理化学』 p.29
- ^ a b c d 『化学・生命科学系のための物理化学』 p.30
- ^ a b c 『理工系学生のための化学基礎』 p.18
参考文献
- 文部省・日本物理学会編 編『学術用語集 物理学編』(増訂版)培風館、1990年9月。ASIN 4563021954。ISBN 4-563-02195-4。 NCID BN05183934。OCLC 23241821。全国書誌番号:90057219。
- P. W. Atkins 著、千原秀昭・中村亘男 訳「1.3. 気体の運動論モデル」『アトキンス物理化学』 上巻(第6版)、東京化学同人、2001年1月30日。ASIN 4807905295。ISBN 4-8079-0529-5。 NCID BA50699995。OCLC 834997205。全国書誌番号:20141197。
- Raymond Chang 著、岩澤康裕・北川禎三・濱口宏夫 訳「3.4. マクスウェル分布則」『化学・生命科学系のための物理化学』東京化学同人、2003年1月10日。ASIN 4807905635。ISBN 978-4-8079-0563-8。 NCID BA60479780。OCLC 676444896。全国書誌番号:20370378。http://www.tkd-pbl.com/book/b16264.html。
- 卜部和夫、川泉文男、平澤政廣、松井恒雄 著「1.3. 気体分子運動論」、野村浩康・川泉文男(編) 編『理工系学生のための化学基礎』(第6版)学術図書出版社、2013年10月31日。ASIN 478060351X。ISBN 978-4-7806-0351-4。 NCID BB13985110。OCLC 867490860。全国書誌番号:22331758。http://www.gakujutsu.co.jp/mybooks/ISBN978-4-7806-0351-4.html。
関連項目

外部リンク
- 法則の辞典『マクスウェル分布』 - コトバンク
- 法則の辞典『マクスウェル‐ボルツマンの速度分布則』 - コトバンク
- 世界大百科事典 第2版『マクスウェル=ボルツマン分布』 - コトバンク
- 日本大百科全書(ニッポニカ)『マクスウェル‐ボルツマン統計』 - コトバンク
- 表示
- 編集
 | この項目は、物理学に関連した書きかけの項目です。この項目を加筆・訂正などしてくださる協力者を求めています(プロジェクト:物理学/Portal:物理学)。 |
- 表示
- 編集





























